熱力学第1法則

木を切った直後のノコギリが温かいのは、仕事が熱に変化したためだ。仕事とエネルギーが変換されることは第1編で学んだが、今回はこの関係を発展させて、これに熱を加えて考えてみよう。
内部エネルギー

あらゆる物体は原子や分子などの小さな粒子からできていて、温度が高いほど熱運動が激しいのであった。熱運動が激しいということは、それだけ物体がエネルギーをたくさん持っていると考えることができて、これを内部エネルギーといって、U〔J〕と表す。今後は主として気体の内部エネルギーを考えていこう。
ポイントは温度Tと内部エネルギーUを関連付けて覚えること。例えば、「内部エネルギーが大きい」ということは、「温度が高い」ということで、「内部エネルギーが小さい」ということは「温度が低い」ということなのだ。
|
温度T |
高い |
低い |
| 内部エネルギーU |
大きい |
小さい |
また、温度変化ΔTと、内部エネルギーの変化ΔUも対応させて覚えよう。温度が上昇すると内部エネルギーは増加するし、温度が低下すると内部エネルギーは減少する。
| 温度変化ΔT |
上昇
ΔT>0 |
低下
ΔT<0 |
|
内部エネルギーの変化ΔU |
増加
ΔU>0 |
減少
ΔU<0 |
上の表にまとめたように、今後は数値が増えることを変化量(ΔT, ΔU)が正、数値が減ることを変化量が負と表現することにする。
気体がした仕事

エネルギーの話が出たので、次は仕事の話をしよう。容器内の気体がピストンを押して外向きに動かしたとき、「気体が外部に仕事をした」という。また、ピストンが内向きに動いたとき、「気体は外部から仕事をされた」という。
ポイントは体積変化ΔVと気体がした仕事Wを対応させて覚えること。気体の体積が増加したとき「気体は仕事をした」といい、気体の体積が減少したとき「気体は仕事をされた」というのだ。
|
体積変化ΔV |
増加
ΔV>0 |
減少
ΔV<0 |
| 気体がした仕事W |
した
W>0 |
された
W<0 |
熱力学第1法則
さあ、いよいよ熱とエネルギーと仕事の関係を見ていくことにしよう。難しそうだが、話はとっても簡単だ。
-
気体に熱を加えると、体積が増えて温度は上がる。
ということが分かっていればそれだけでいい。
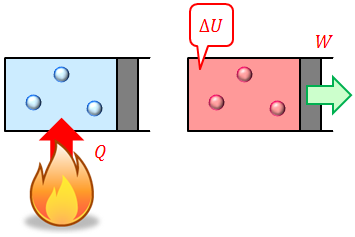
まず、気体に熱を加えるということは「気体が熱を吸収する」ということだから、このとき気体が吸収した熱量をQ〔J〕とする。また、気体の体積が増えるということは「気体が外部へ仕事をした」ということだから、このときに気体がした仕事をW〔J〕とする。さらに、気体の温度が上がるということは「気体の内部エネルギーが増加した」ということだったから、このとき増加した内部エネルギーをΔU〔J〕とすれば、今の話は、
-
熱量Qを吸収した気体は、外部へ仕事Wをして内部エネルギーもΔUだけ増加する。
と言い換えることができる。これは、吸収した熱量Q〔J〕の一部が仕事W〔J〕として使われ、余りが内部エネルギーU〔J〕として蓄えられるということなので、

という関係が成り立っていることになる。エネルギーは熱や仕事に形を変えながらも保存されているのだ。この、広い意味でのエネルギー保存則が成り立つことを熱力学第一法則という。

気を付けなくてはならないのは、Q,W,ΔUの正負だ。例えば、
- 気体から熱を奪うと、気体の体積が減って温度は下がる。
という内容の場合、
- 気体が熱を放出→気体が吸収した熱量Qは負
- 気体が仕事をされた→気体がした仕事Wは負
- 気体の内部エネルギー減少→内部エネルギーの変化ΔUは負
である。
| 気体が吸収した熱量Q |
吸収
Q>0 |
放出
Q<0 |
| 気体がした仕事W |
した
W>0 |
された
W<0 |
|
内部エネルギーの変化ΔU |
増加
ΔU>0 |
減少
ΔU<0 |
気体の状態変化

気体の体積が変わらないような状況で熱を加えると、加えた熱量Qがそのまま内部エネルギーの増加ΔUとなる。

このような変化を定積変化という。

気体の圧力が変わらないように熱を加えてやると、加えた熱量Qの一部が仕事Wとして消費され、残りが内部エネルギーの変化ΔUとなる。
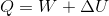
このような変化を定圧変化という。

気体の温度が変わらないように熱を加えてやると、加えた熱量Q
がすべて仕事Wとして消費され、内部エネルギーは変化しない。
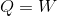
このような変化を等温変化という。温度Tが一定のとき、圧力pと体積Vが反比例の関係にあることは、ボイルの法則と呼ばれている。また、気体の状態方程式
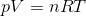
より、温度Tが高いほどグラフの面積pVが大きくなることが分かるので、原点から離れているほど高温状態を表していることになる。
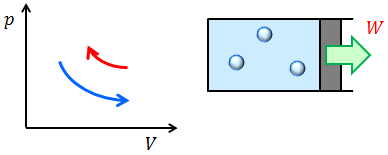
外部との熱のやり取りがないように体積を増やすと温度が下がる。これは、気体が仕事をして内部エネルギーが減少したことを意味している(W>0, ΔU<0)。
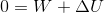
このような変化を断熱変化という。
